课程内容
第六单元《碳和碳的氧化物》课题2 二氧化碳制取的研究
探究:实验室制取二氧化碳所用的反应物
一、药品及反应原理
实验编号
实验药品
实验现象
实验分析
1
碳酸钠和稀盐酸
大量气泡
反应很快 不适宜
2
石灰石和稀盐酸
许多起泡
速度适中 适合
3
石灰石和稀硫酸
少量气泡
一会儿停止 不适宜
1、药品:石灰石(或大理石)和稀盐酸
↓
(主要成分为CaCO3)
说明
(1)不能用稀硫酸代替稀盐酸。因为发生如下反应:【CaCO3+H2SO4=CaSO4+H2O+CO2↑】,生成的硫酸钙微溶于水,它覆盖在碳酸钙表面,阻止了反应的继续进行。
(2)不能用浓盐酸。因为浓盐酸具有较强的挥发性,易挥发出氯化氢气体,导致收集的二氧化碳气体不纯。
(3)不能用碳酸钠代替碳酸钙。因为碳酸钠和稀盐酸反应速度太快、不易控制。
2、反应原理:
CaCO3+2HCl==H2CO3+CaCl2
碳酸 氯化钙
H2CO3==H2O+CO2↑
总反应:CaCO3+2HCl==CaCl2+H2O+CO2↑
二、装置的确定
实验室制氧气的装置:
第1种方法: 第2种方法:
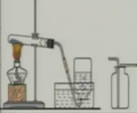
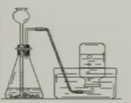
2KMnO4 K2MnO4+MnO2+O2↑ 2H2O2
K2MnO4+MnO2+O2↑ 2H2O2 2H2O+O2↑
2H2O+O2↑
请同学们思考以下几个问题:
1、实验室制取气体的装置由哪几部分组成?
两部分组成:发生装置和收集装置
2、确定气体发生装置时应考虑哪些因素?
(1)反应物的状态(如液态、固态)
(2)反应条件(如加热、不加热等)
3、收集气体一般有哪些方法?
一般有两种:
(1)排空气法:①向上排空气法
②向下排空气法
(2)排水法
4、确定收集装置时应考虑哪些因素?
主要应以两个物理性质方面去考虑:
(1)气体的密度与空气密度比较
(2)气体在水中的溶解性
小结:实验室里制取气体的装置包括:


二氧化碳和氧气制取实验及相关性质比较
选择以下仪器设计制取二氧化碳的装置:
反应物的状态
反应条件
气体的密度比空气的大或小
是否溶于水
是否与水反应
CO2
固+液
常温
大
能
O2
固+液(H2O2和MnO2)
或固(KMnO4) 常温
加热 稍大
不易
针筒 锥形瓶 平底烧瓶 烧杯 试管 集气瓶 分液漏斗
长颈漏斗 导管 水槽 酒精灯
注意:便于加酸并控制反应速度
二、实验装置的确定:
1、发生装置:固+液不加热型(长颈漏斗一定要插入液面以下)
2、收集装置:向上排空气法
3、制取二氧化碳的具体装置图
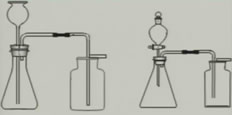
三、实验室制取CO2的步骤:
(1)检查装置的气密性;
(2)加入药品(先向固后液);
(3)收集气体。
四、CO2的检验和验满:
1、检验方法:将产生的气体通入澄清的石灰水,若石灰水变浑浊,证明生成的气体是CO2。
2、验满方法:将燃着的木条伸到集气瓶口,木条熄灭,则说明已满。
课堂练习
1、已知氨气是一种无色有刺激性气味的气体,密度小于空气,极易溶于水。实验室常用碱石灰和硫酸铵两种固体混合加热的方法制取氨气。根据所学的知识判断,实验室制取氨气时发生装置应选择( )装置,收集装置( )装置。
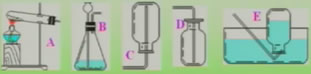
课堂练习
1、实验室制取CO2和O2的共同点是( )
A、气体发生装置相同 B、都可以用向上排空气法收集
C、反应时都需要加热 D、都可以用排水法收集
2、实验室制取二氧化碳需要用的一组药品是( )
A、大理石和稀盐酸 B、石灰石和稀硫酸
C、木炭和氧气 D、碳酸钠和稀硫酸
3、证明集气瓶中收满二氧化碳的正确方法是( )
A、加入澄清石灰水
B、加入紫色石蕊试液
C、把燃着的木条放在集气瓶口
D、把燃着的木条伸到集气瓶内
4、实验室制取二氧化碳一般有五个步骤:
①检验装置气密性
②按要求装配好仪器
③向长颈漏斗中注入稀盐酸
④收集气体
⑤向广口瓶中放入几小块大理石
其中正确的顺序是( )
A、①②③④⑤ B、②①⑤③④
C、②①③④⑤ D、③④⑤②①
5、下列制取二氧化碳的装置有哪些错误?
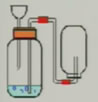
6、硫化氢气体是一种有毒气体,它能溶于水,密度比空气的大。实验室常用硫化亚铁(固)与稀硫酸溶液反应制硫化氢气体。则制取装置可选用下列哪套装置?收集硫化氢气体该用什么方法收集?为什么?能否用排水法?为什么?
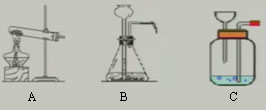
此内容正在抓紧时间编辑中,请耐心等待
崔老师
女,中教高级职称
优秀教师。多次被评为市教育局“教学标兵”,教学功底扎实,教学经验丰富。
























