课程内容
第九单元《溶液》课题3 溶液的浓度(一)
在亚洲西部,巴勒斯坦和约旦交界处,有一个“死海”。远远望去,死海的波涛此起彼伏,无边无际。但是,谁能想到,如此浩荡的海水中竟没有鱼虾、东草,甚至连海边也寸草不生?这大概就是“死海”得名的原因吧。然而,令人惊叹的是,人们在这无鱼无草的海水里,竟能自由游弋;即使是不会游泳的人,也总是浮在水面上,不用担心会被淹死。真是“死海不死”。那么死海的海水与其他海水在组成上有什么不同呢?
你知道下面瓶中标签是什么意思吗?
化学纯 500mL
浓盐酸(HCl)
含HCl 37%
密度为1.18g/cm3
下面我们就来学习溶液组成的表示方法。
实验9-7:分别向20mL水中各加入0.1克、0.5克、2克硫酸铜,比较三种溶液的颜色,哪种溶液最浓?哪种溶液最稀?你判断的依据是什么?
在三支试管中各加入20mL水,然后分别加入约0.1g、0.5g、2g固体硫酸铜。比较三种溶液的颜色。
| 试管编号 |
溶液颜色比较 |
溶剂质量/g |
溶质质量/g |
溶液质量/g |
| 1 |
浅 |
20g |
0.1g |
20.1g |
| 2 |
较深 |
20g |
0.5g |
20.5g |
| 3 |
深 |
20g |
2g |
22g |
农夫自杀 只因果树离奇死亡
据《扬子晚报》报道:2009年7月20日,河南一果农,因用自己全部家当种植的果树离奇死亡而伤心过度,果农自尽而死,据其家人介绍,他本人不大识字,7月18日晚买来了250千克的液体肥料,他掺入了1000千克的水后进行喷洒两天后,所有果树离奇死亡。
在使用溶液时必须确切知道溶液的浓度。表示溶液浓度的方法有很多,最常用的是溶液的质量分数。
知识点一:溶质质量分数
1、定义:是溶质质量和溶液质量之比。
2、公式:
溶质质量分数=溶质质量/溶液质量×100%
溶质的质量=溶液质量×溶质质量分数
溶质的质量=溶质质量÷溶质质量分数
在三支试管中各加入20mL水,然后分别加入约0.1g、0.5g、2g固体硫酸铜。比较三种溶液的颜色。
| 试管编号 |
溶液颜色比较 |
溶剂质量/g |
溶质质量/g |
溶液质量/g |
溶质质量分数 |
| 1 |
浅 |
20g |
0.1g |
20.1g |
0.49% |
| 2 |
较深 |
20g |
0.5g |
20.5g |
2.43% |
| 3 |
深 |
20g |
2g |
22g |
9.09% |
溶质的质量分数(通常以百分数表示)
定义:溶质的质量与溶液的质量之比
溶质的质量分数=溶质质量/溶液质量×100%
或=溶质质量/(溶质质量+溶剂质量)×100%
注意:
①溶液的质量=溶质的质量+溶剂的质量
无溶入溶液的不计。
②计算时上下质量单位要统一。
③不要忘记×100%,最后得到百分数。
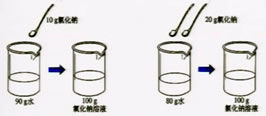
[实验9-8]
两杯溶液都是无色透明,怎样比较溶液的浓稀?
| 溶质质量/g |
溶剂(水)质量/g |
现象 |
溶液中溶质的质量分数 |
| 10 |
90 |
固体溶解 |
10% |
| 20 |
80 |
固体溶解 |
20% |
结论:溶液中溶质的质量分数越大,溶液浓度越大。
[讨论]某氯化钠溶液中溶质的质量分数为10%,其含义是什么?
①表示100份质量的氯化钠溶液中含有10份质量的氯化钠,90份质量的水。
②溶质质量:溶剂质量=1:9
资料卡片:体积分数
除质量分数以外,人们有时也用体积分数来表示溶液的浓度。例如用作消毒剂的医用酒精中乙醇的体积分数为75%,就是指每100体积的医用酒精中含75体积的乙醇。你还能举出其他用体积分数来表示浓度的例子吗?
知识点二:溶质质量分数计算
[题型一]:有关溶质、溶剂和溶液之间的换算
计算的依据:
溶质质量分数=溶质质量/溶液质量×100%
溶液质量=溶质质量+溶剂质量
【例题1】在农业生产中,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150kg这种溶液,需要氯化钠和水的质量各是多少?
【解】溶质的质量分数=溶质质量/溶液质量×100%
溶质质量=溶液质量×溶质的质量分数
=150kg×16%=24kg
溶剂质量=溶液质量-溶质质量
=150kg-24kg=126kg
答:配制150kg质量分数为16%的氯化钠溶液需24kg氯化钠和126kg水。
练习1(课本P45)某温度时,蒸干35g氯化钾溶液,得到7g氯化钾,求该溶液中溶质的质量分数。
练习2、20g 10%的盐水中放入2g水或2g食盐,求:所得溶液的溶质质量分数。
练习3、20g 10%的盐水中倒出一半,求:剩余溶液的溶质的质量分数。
溶质质量分数与溶解度的比较
溶质的质量分数36%是指:100g溶液中含有36g溶质。
溶质T℃时溶解度36g是指:在T℃时,100g水最多溶解该溶质36g。
饱和溶液的溶质质量分数=溶解度/(100g+溶解度)×100%
在一定温度下的饱和溶液是最浓的溶液。
[题型二]:一定温度时饱和溶液中溶质的质量分数计算
计算的依据:
一定温度时饱和溶液的溶质质量分数=溶解度/(100g+溶解度)×100%
例2、已知20℃时食盐的溶解度为36g,求20℃时食盐饱和溶液的溶质质量分数。
解:20℃时食盐饱和溶液的溶质质量分数为
36g/(100g+36g)×100%=26.5%
答:20℃时食盐饱和溶液的溶质质量分数为26.5%。
判断
小明说:“我在20℃时配制了一瓶质量分数为30%的氯化钠溶液。”小刚说:“这是不可能的。”哪个同学说得对呢?(已知20℃时食盐的溶解度为36g)
20℃时饱和氯化钠溶液中溶质的质量分数为:
36g/(100g+36g)×100%=26.5%
练习4(课本P45)在20℃时,将40g硝酸钾固体加入100g水中,充分搅拌后,仍有8.4g硝酸钾固未溶解。请填写下列空白:
①所得溶液是20℃时硝酸钾的______溶液;(填“饱和”或“不饱”)
②20℃时硝酸钾的溶解度为______;
③所得溶液中硝酸钾的质量分数为______。
练习5:10℃时,NaCl的溶解度是36克。现有50克水放入20克NaCl固体,求:所得溶液的溶质质量分数。
小结
溶液组成的表示方法——溶质质量分数
1、定义:溶质的质量与溶液的质量之比
2、两个计算公式
溶质的质量分数=溶质质量/溶液质量×100%
饱和溶液的溶质质量分数=溶解度/(100g+溶解度)×100%
(只适用于一定温度下的饱和溶液)